Физический энциклопедический словарь - ван-де-граафа генератор
Ван-де-граафа генератор
ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ,
одно из первых уравнений состояния реального газа. Предложено в 1873 голл. физиком Я. Д. Ван-дер-Ваальсом (J. D. van der Waals). Для моля газа, имеющего объём V при темп-ре Т и давлении р, имеет вид:
(p+a/V2)(V-b)=RT,
где R — универсальная газовая постоянная, а a и b — эксперим. константы, учитывающие отклонение св-в реального газа от св-в идеального. Так, член a/V2 имеет размерность давления и учитывает притяжение молекул в результате межмолекулярного взаимодействия, а константа b — поправка на собств. объём молекул, учитывающая отталкивание молекул на близких расстояниях. При больших V (а также для разреж. газов) константами а и & можно пренебречь и В. у. переходит в ур-ние состояния идеального газа (см. Клапейрона уравнение).
В. у. явл. приближённым и количественно определяет св-ва реальных газов лишь в области высоких Т и низких р. Однако качественно оно позволяет описывать поведение газа при высоких р, конденсацию газа и критич. состояние.
На рисунке приведены изотермы, рассчитанные по В. у. При низких Т все три корня В. у.— действительные, а выше критич. темп-ры (Тк) остаётся лишь один действит. корень. Это означает, что при Т>ТК в-во может находиться только в одном (газообразном) состоянии, а при Т<ТК — в трёх состояниях (двух стабильных — жидком Vж и газообразном Vг — и одном нестабильном). Точки прямой ас отвечают равновесию жидкости и её насыщ. пара. В условиях равновесия, напр. в состоянии, соответствующем точке b, относит, кол-ва жидкости и пара определяются отношением отрезков вс/ва («правило моментов»). Равновесию фаз при определ. Т соответствует давление насыщ. пара рнп и интервал объёмов отVж до Vr.
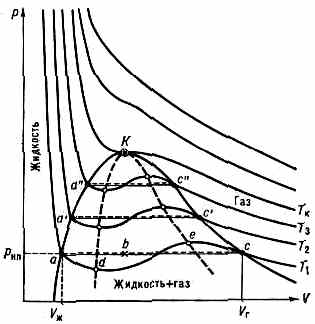
Диаграмма состояния в-ва в координатах р — V: t1, Т2, Т3, Тк — изотермы, рассчитанные по ур-нию Ван-дер-Ваальса; К — критич. точка. Линия dKe (спинодаль) очерчивает область неустойчивых состояний.
При более низких р (за областью, где возможно одновременное существование газа и жидкости) изотерма характеризует св-ва газа. Левая, почти вертик. часть изотермы отражает малую сжимаемость жидкости. Участки ad и еc (и аналогичные участки др. изотерм) относятся соотв. к перегретой жидкости и переохлаждённому пару (метастабильные состояния). Участок de физически неосуществим, т. к. здесь происходит увеличение V при увеличении р. Совокупность точек а, а', а" и с, с', с", . . . определяет кривую, наз. бинодалью, к-рая очерчивает область совместного существования газа и жидкости. В критич. точке К параметры Тк, рк и Vк имеют значения, характерные для данного в-ва. Однако если в В. у. ввести относит. величины Т/Тк, р/рк и V/VK, то можно получить т. н. приведённое В. у., к-рое явл. универсальным.

Вопрос-ответ:
Самые популярные термины
1 | 1380 | |
2 | 1051 | |
3 | 994 | |
4 | 943 | |
5 | 925 | |
6 | 827 | |
7 | 801 | |
8 | 801 | |
9 | 712 | |
10 | 709 | |
11 | 689 | |
12 | 637 | |
13 | 626 | |
14 | 614 | |
15 | 533 | |
16 | 523 | |
17 | 517 | |
18 | 501 | |
19 | 483 | |
20 | 479 |










